2026-05-06
导读
琥珀酸半醛脱氢酶缺乏症(SSADHD)是一种罕见且致死的神经遗传与代谢疾病,目前无有效治愈药物。传统的病理观念往往认为,这类神经发育障碍在发病后造成的损伤难以逆转。然而,近期发表了题为“Postnatal gene restoration in succinic semialdehyde dehydrogenase deficiency (SSADHD) reveals phenotype reversibility”的最新研究成果。该研究开发了全新的小鼠模型,并证实即便在疾病出现严重症状后才进行基因替代治疗,SSADHD的严重表型依然可以被有效逆转,这为未来的临床转化提供了强有力的概念验证。
1.ALDH5A1基因突变导致神经递质代谢崩溃,现有疗法均告失败
SSADHD是由ALDH5A1基因的突变丧失功能所引起的常染色体隐性代谢异常。该基因主要负责编码琥珀酸半醛脱氢酶(SSADH),这是人体大脑中主要的抑制性神经递质——γ-氨基丁酸(GABA)降解过程中的关键酶。
当该酶由于基因缺陷而缺乏时,GABA及其代谢副产物γ-羟基丁酸(GHB)会在体内发生严重的病理性积累。这种代谢毒性积累会导致患者出现深刻的神经系统与发育迟缓症状。约50%的患者会患上癫痫,甚至在青春期或成年期面临猝死(SUDEP)的风险;此外,患者还伴有共济失调、自闭症等特征,约10%的患者甚至完全失去语言能力并终生依赖轮椅。
面对这一顽疾,现有的治疗手段显得束手无策。针对行为症状和癫痫的药物通常具有严重的抗药性。过去的三项临床靶向药物试验,最终都因毒性无法耐受或毫无临床益处而宣告失败。此外,由于重组蛋白半衰期短且难以穿透血脑屏障,实验性的酶替代疗法(ERT)疗效也十分有限。因此,能够在大脑中靶向恢复基因功能的基因替代疗法,成为了攻克该疾病的核心方向。
2.新型诱导型小鼠模型证实:断奶期发病后,疾病表型仍可逆转
在全面推进基因治疗前,必须明确一个根本问题:如果在出生后甚至已经出现明显症状时才恢复基因功能,能否扭转疾病的进程?
为此,研究团队利用技术构建了一种全新的诱导型小鼠模型:Aldh5a1lox-STOP小鼠。在自然状态下,纯合子(Hom)突变小鼠的该基因完全失活,完全再现了人类重度SSADHD患者的病理表现:它们体重不达标、表现出病态的极度活跃,血液中的GHB浓度更是比正常野生型(WT)小鼠高出50多倍,且寿命极短,平均在出生后22天左右就会死亡。
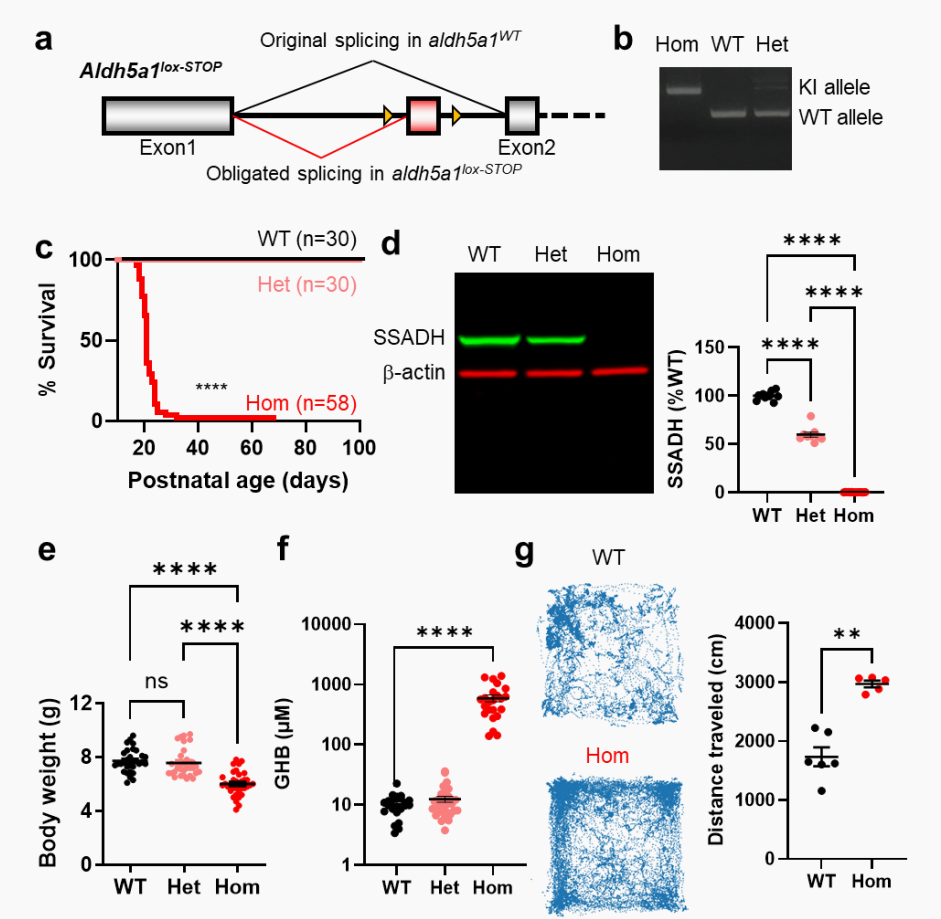
图1 Aldh5a1lox-STOP小鼠模型的构建与基线特征分析
图1展示了Aldh5a1lox-STOP小鼠模型的构建方式、纯合子小鼠极低的生存率、缺失的SSADH蛋白质表达以及异常升高的血液GHB水平。
研究人员在小鼠出生后第16天(P16,此时小鼠已经表现出明显的症状,大致相当于人类的幼儿或青春期前阶段)进行了干预。他们通过静脉系统注射了一种能够穿透血脑屏障的腺相关病毒载体(AAV-PHP.eB-Cre),利用Cre重组酶精准去除了导致基因失活的终止序列,从而在小鼠的全身及大脑中恢复了内源性Aldh5a1基因的表达。
结果极其显著:未受治疗的纯合子小鼠在早期全部死亡,而接受AAV-Cre治疗的小鼠中,高达89%(16/18只)存活到了90天以上。治疗不仅挽救了生命,小鼠的体重恢复至与正常小鼠无异的水平,致病性GHB水平大幅下降,异常的多动行为也完全正常化。这一数据确凿证明:即使在疾病的症状期恢复大脑的基因表达,SSADHD的致命表型依然是可逆转的。
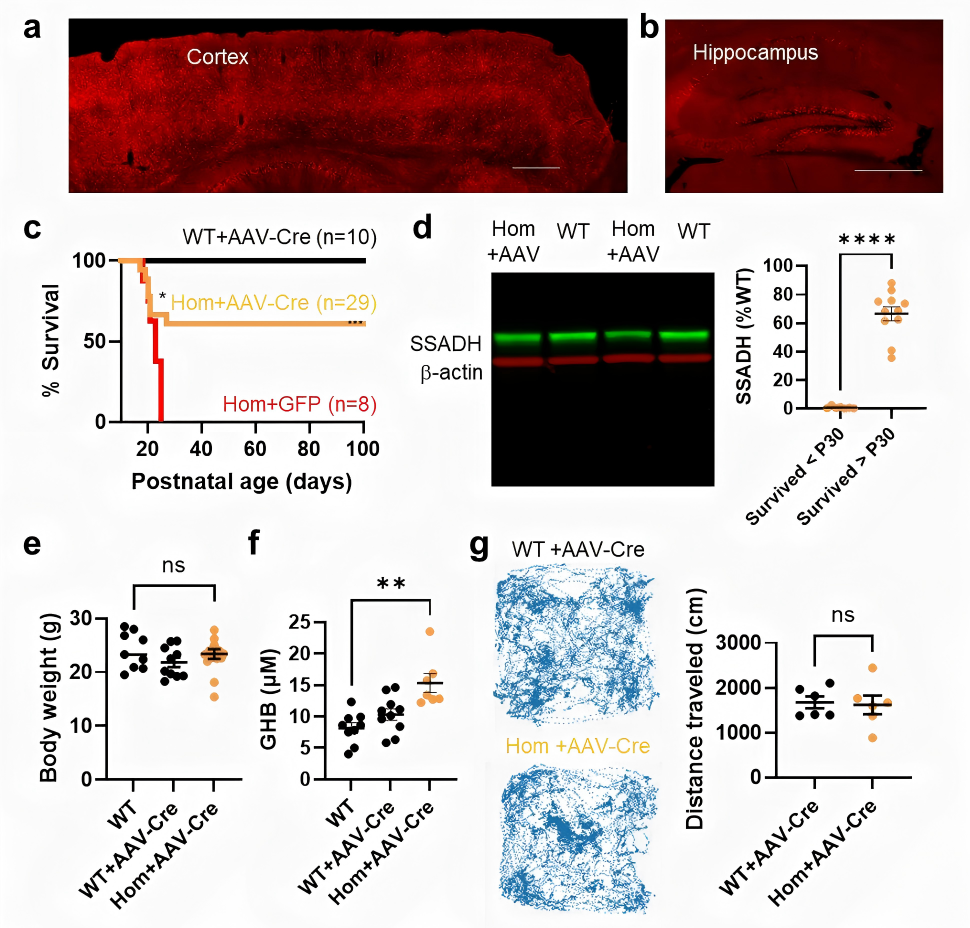
图2AAV介导Aldh5a1lox-STOP小鼠全脑Aldh5a1基因功能重建
图2展示了AAV-Cre介导的大脑基因恢复后,小鼠生存率的飙升、大脑皮层蛋白质的恢复以及异常运动行为的正常化。
3.临床转化曙光:新型AAV基因疗法显著提高生存率并改善代谢
在确认了疾病的可逆性之后,研究团队进一步设计了一款高度贴近未来临床应用的新型AAV治疗载体。
为了降低基因过度表达可能带来的副作用(例如过度清除突触内的GABA),他们设计了一个包含人类ALDH5A1功能性天然启动子(FLnP)以及人类ALDH5A1全长编码序列的重组AAV载体(即AAV-FLnP-hALDH5A1)。天然启动子能够模拟体内的自然表达模式,以降低脱靶效应的风险。
研究团队将这款新型疗法同样注射到处于发病期(P16)的突变小鼠体内。实验结果揭示了几个关键结论:
生存期显著改善:60%的治疗小鼠存活超过了90天,远远突破了未治疗小鼠22天的生命极限。
明确的蛋白质起效阈值:研究发现,小鼠的存活率与大脑中恢复的SSADH蛋白数量呈直接的正相关关系。只要蛋白质表达恢复到野生型的40%以上,就能带来生长的改善和存活率的大幅提升。
生物标志物响应:尽管通过AAV治疗后小鼠的GHB水平比完全健康的小鼠略高(约1.5倍),但这种残留浓度(约19.13μM)已经安全落入了正常人类的基准范围(<49μM),表明这种程度的GHB水平在体内是完全可以耐受的。
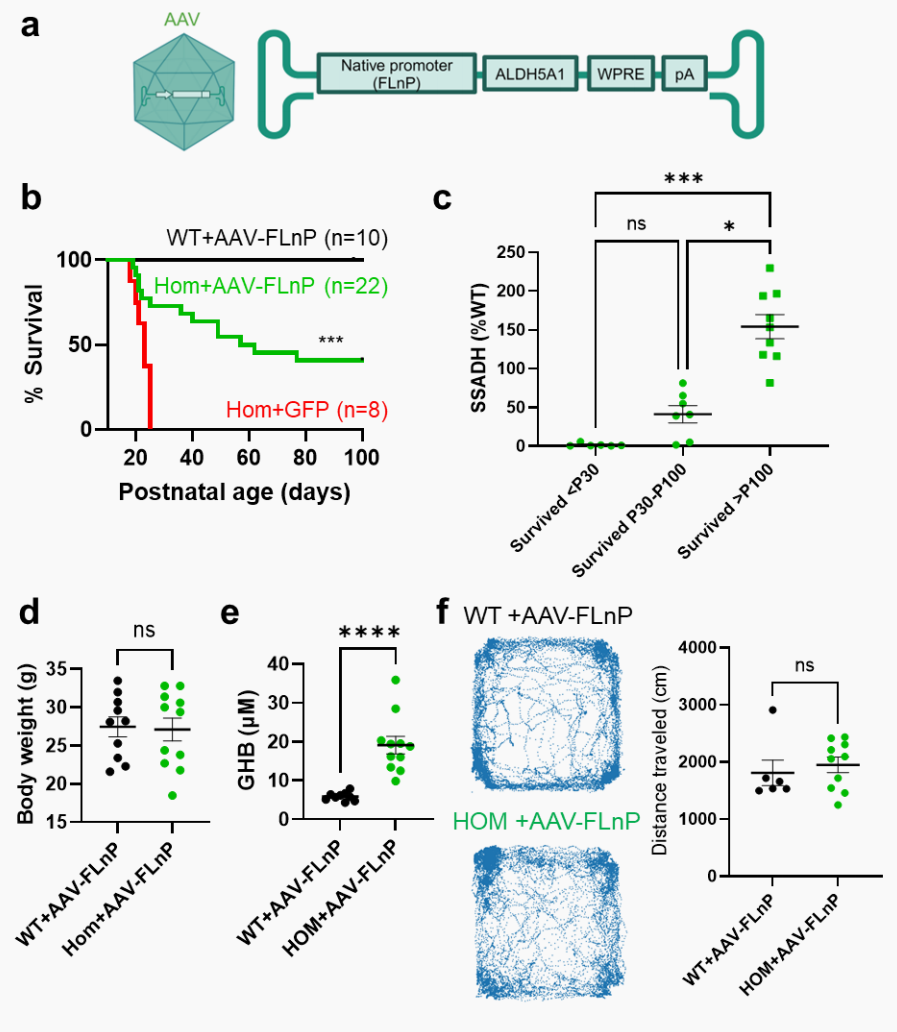
图3 AAV-PHP.eB-CMV-Cre介导的全脑范围转基因表达
图3展示了针对SSADHD的AAV基因治疗候选药物的设计图,以及治疗后小鼠存活率的提高、SSADH蛋白质恢复水平与存活的强正相关性。
4.跨越“不可逆”的传统认知,为罕见病治疗提供新思路
长期以来,在神经发育疾病领域存在一种担忧:胚胎期就开始的异常代谢物(如高GABA和GHB)暴露,可能早就给大脑细胞和回路留下了不可逆的损害。然而,这项研究通过严谨的小鼠模型数据表明,当在接近人类幼童期的症状阶段介入传递该基因,依然可以逆转致死性、异常行为及毒性代谢物积累等核心病理。
该研究不仅证明了同时覆盖大脑和外周系统的AAV基因替代疗法具有现实可行性,更为未来的临床试验确立了清晰的靶点指标(>40%的蛋白恢复),并验证了血液GHB可作为衡量疗效和靶点接合度的重要机制生物标志物。这为最终将SSADHD基因疗法推向临床人体试验搭建了坚实的转化桥梁。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。